ESTADOS DE LA MATERIA
La
materia se presenta de varias maneras y formas. El color, el olor y la
textura son propiedades de la materia que nos ayudan a diferenciarlos. Llamamos estado a la manera en que se presenta la materia. Estos pueden ser:
Sólido: tiene una
forma definida, como la madera y el cobre.
Sus moléculas no cambian de posición.
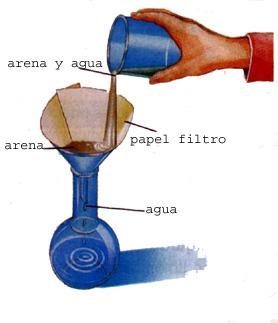
Líquido: no tiene una forma definida, como el agua y el
aceite. Sus moléculas pueden cambiar de posición.
Gaseoso: no tiene una forma definida, como el aire y el vapor
de agua. Sus moléculas cambian
libremente de posición.
Plasma: tampoco tiene una forma definida, un tipo de gas ionizado que sólo existe de forma natural en el sol, estrellas y en el espacio sideral o en condiciones especiales en la tierra. Dependiendo las condiciones, la materia puede presentarse en uno u otro estado.
Plasma: tampoco tiene una forma definida, un tipo de gas ionizado que sólo existe de forma natural en el sol, estrellas y en el espacio sideral o en condiciones especiales en la tierra. Dependiendo las condiciones, la materia puede presentarse en uno u otro estado.